複数のモノマーを用いてラジカル重合を行う場合、得られるポリマーのモノマー配列はモノマーの反応性によって変化します。
例えば、スチレンと酢酸ビニルを仕込みモノマー比率1:1でラジカル共重合した場合には、重合初期はスチレンを多く含んだポリマーが生成し、スチレンがほぼ消費されると酢酸ビニルを多く含んだポリマーが生成します。
このような現象が起こる理由は「モノマーの反応性比」という概念で説明がなされます。
この記事では、モノマーの反応性比について解説していきます。
ラジカル共重合におけるモノマーの消費速度
ラジカル共重合では成長反応の反応速度は単独重合に比べて複雑になります。
成長ラジカルはモノマーごとに違い種になりますし、反応するモノマーもモノマーの種類だけあることになります。
ここでは2種類のモノマーM1とM2の共重合を行う場合を考えていきます。
この場合には成長反応は以下の4つの式となります。
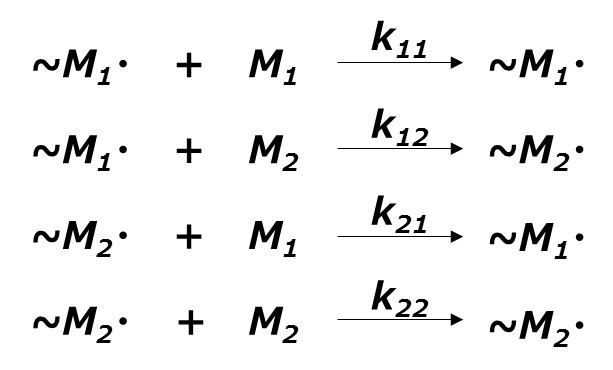
反応速度定数はそれぞれk11, k12, k21, k22とします。(ラジカルの反応性は末端構造だけで決まると仮定しています。)
このときのモノマーM1とM2の瞬間的な消費速度が分かれば、共重合物中の瞬間的なモノマーM1とM2の組成比が分かります。
そこでM1とM2の瞬間的な消費速度(d[M1]/dt、d[M2]dt)について式を立てると以下にようになります。
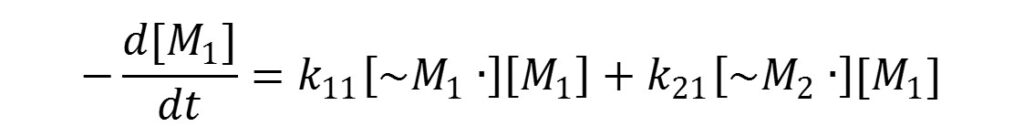
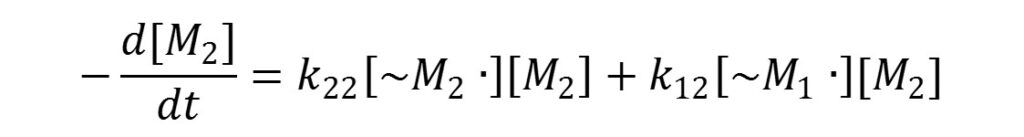
これらの式から、以下のようにM1とM2の消費速度の式が導出できます。

また、瞬間的な各モノマー末端のラジカル濃度、(すなわちM1・とM2・)の濃度は変化しない状態と仮定できます。(定常状態近似)
上の4つの反応式中のM1とM2のラジカル濃度が変化する式はM1・とM2の反応、M2・とM1の反応です。
このため、以下のように式を書くことができます。

この式をM1とM2の消費速度の式に代入することで、ラジカル濃度の項を消去できます。(M2・を消すように代入すると分子分母の各項に[M1・]が出てくるので約分できます。)
そして、r1=k11/k12, r2=k22/k21と置くと以下の式が導かれます。
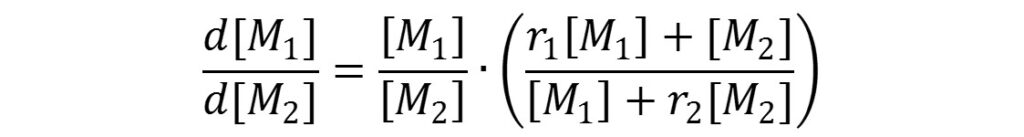
この式は共重合組成式やMayo-Lewis式(メイヨー・ルイス式)と呼ばれており、モノマーM1とM2のある濃度のときに得られるポリマー中の共重合組成比を表しています。
r1とr2はモノマー反応性比と呼ばれており、共重合におけるポリマー中の組成比を知るうえで重要なパラメーターです。
反応性比 r1とr2で共重合組成が分かる
ここでもう一度共重合組成式を見てみましょう。
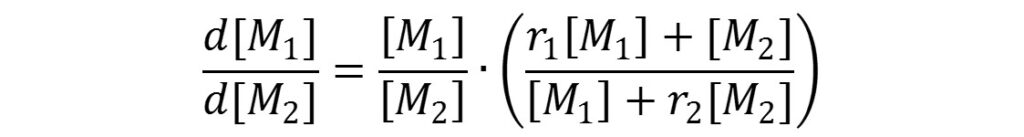
後ろの項がなければ、モノマーの消費速度の比はモノマーの仕込み濃度の比に等しい、という式になっています。
なのでr1=r2=1とした場合は後ろの項が約分されて1となるので、モノマー濃度の比=モノマー消費量の比となります。
またr1=k11/k12=1, r2=k22/k21=1なので、末端の成長ラジカルのM1への反応速度とM2への反応速度が同じになります。
このため、共重合組成中のモノマー組成比は仕込みモノマー濃度と同じとなり、かつモノマー配列は完全にランダムになります。
このような重合のことを理想共重合もしくはランダム共重合)という。
このようにr1とr2が分かれば、モノマー仕込み比に対するモノマー消費速度が分かり、同時にそれぞれのモノマーがもう片方のモノマーとどれくらい反応しやすいかが分かるわけです。
①r1=r2=1の場合はランダム共重合
上で紹介した通り、r1=r2=1の場合はモノマーの仕込み濃度の等しい組成で、ランダム共重合体が得られます。
②r1=r2=0の場合は交互共重合
つぎにr1=r2=0の場合ですが、k11=k22=0なので同じモノマー同士では反応せず、もう片方のモノマーと必ず反応します。
そしてM1とM2の消費速度は仕込み濃度に依らず等しくなります。
すなわちモノマー仕込み濃度の比に関係なく、-M1-M2-M1-M2-M1-M2-という完全に交互なモノマー配列となったポリマーが得られます。
このような重合は交互共重合と呼ばれています。
③r1<1, r2<1の場合は交互に反応しやすい共重合
r1<1, r2<1の場合は成長末端のラジカルはいずれももう片方のモノマーへの反応が起こりやすい場合です。
例えば、スチレンと無水マレイン酸の共重合はこのパターンに当てはまります。
このようなケースでは、共重合の組成はモノマー仕込み比よりも仕込みモノマーが1:1になる側に近づいたポリマー組成が得られます。
また、M1の仕込み比に対してポリマー中のM1をプロットするとランダム共重合でのプロットと交差します。
この交点での組成は、モノマーM1仕込み濃度とポリマー中のM1の組成比が同じであり、重合率に依らず重合液中のモノマー濃度が変化せず、得られるポリマーの組成も変化しません。
このような組成をアゼオトロープ組成と言います。(アゼオトロープは共沸混合物を意味し、混合物の蒸留において気相と液相の組成濃度が同じとなるとそれ以上に純度を上げることのできない。これに例えて、重合率に依らず組成が変化しない仕込み比をアゼオトロープ組成という)
④r1>1, r2<1の場合はM1を多く含んだポリマーが得られる
r1>1, r2<1の場合はどちらの成長末端もM1への反応が速い場合です。
スチレンと酢酸ビニルの共重合はこのパターンに当てはまります。
このようなケースで、(M1の仕込み濃度が低い場合でも)共重合の組成はM1を多く含んだポリマーが得られます。
冒頭で紹介したスチレンと酢酸ビニルの共重合ですが、スチレンと酢酸ビニルを1:1で仕込んだとしても反応性比から、M1(=スチレン)がほとんどなくなるまではスチレンを多く含んだポリマーが得られ、そしてスチレンが消費されるとM2(=酢酸ビニル)単独での重合が起こるわけです。
まとめ
今回の記事ではモノマーの反応性比について解説しました。
共重合反応においては、反応性比r1とr2から得られる共重合体の組成が分かるため、非常に有用です。
r1とr2のパターンを実際のモノマー組み合わせとセットで覚えておくと、モノマー間の反応性も把握できるので一石二鳥です。

コメント
些細なことで恐縮ではございますが、タイトルが 「共重合”の”おけるモノマー反応性比」 になっていますが、”に” でしょうか?
次のページについてです
https://chem-labo.com/polymer-synthetic-chemistry/reactivity-ratio/
度々 参考にさせて頂いております。いつもありがとうございます。
こちらこそありがとうございます。
タイトルは「に」です。先ほど修正いたしました。